La molécule des protides est constituée d’atomes de carbone (C), d’hydrogène (H), d’oxygène (O) et d’azote (N).
Mise en évidence des protides :
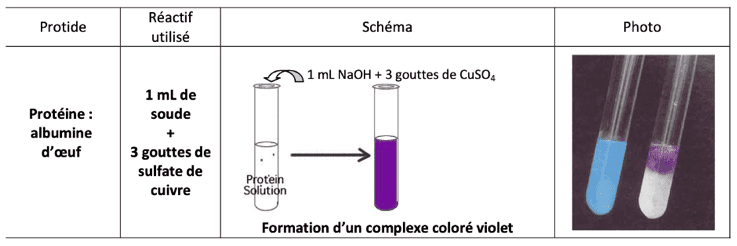
Test de reconnaissance d’un peptide ou d’une protéine (Test du Biuret).
Dans un tube à essai contenant une solution de protéine, on introduit :
- 1 mL d'une solution d’hydroxyde de sodium à 20% (NaOH) ;
- Quelques gouttes de sulfate de cuivre à 1% (CuSO4).
Et observer.
Les acides α-aminés
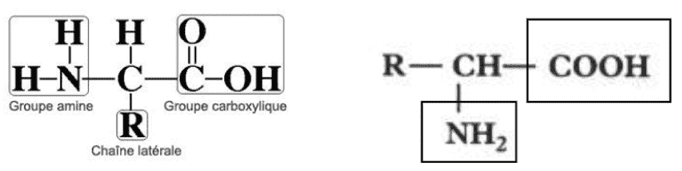
Un acide aminé ou amino-acide est un composé organique possédant à la fois une fonction acide carboxylyque –CO2H et une fonction aminé –NH2.
Un acide α–aminé est un acide carboxylique dans lequel le groupe amino est porté par l’atome de carbone en Ç du groupe carboxyle.
La formule générale des acides αα-aminés naturels est :
H|R–C–COOH|NH2
Où R peut être un atome d’hydrogène, un groupe alkyle linéaire.
Liaison peptidique
Les acides aminés donnent lieu à une grande diversité de combinaisons en biologie parce que ceux-ci peuvent se polymériser : on forme ainsi des polypeptides. De tels polymères se forment à la suite de réactions répétées de la fonction acide carboxylique d’un acide aminé avec le groupe amino d’un autre, ce qui aboutit à l’élaboration d’une chaîne d’amides. Le lien amide qui unit des acides aminés est appelé liaison peptide.
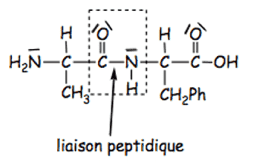
Exemple de dipeptide :
Ce dipeptide est obtenu par condensation de deux acides aminés : l’alanine et la phénylalaline.
Les protéines, constitution et hydrolyse
L’enchaînement d’un nombre élevé d’acides aminés aboutit à la formation d’une protéine. Cette molécule est très longue.
Il est possible de rompre les liaisons peptidiques des protéines par hydrolyse. Dans le corps humain, ce sont des enzymes qui sont responsables de cette réaction.