Une espèce chimique à l'échelle macroscopique est constituée d’un grand nombre d’entités chimiques identiques (atomes, molécules, ions) à l'échelle microscopique.
Un corps pur est constitué d’une seule espèce chimique et un mélange est constitué de plusieurs espèces chimiques.
On distingue les mélanges homogènes (les constituants ne se distinguent pas à l’œil nu) et les mélanges hétérogènes.
Deux liquides sont miscibles s’ils forment un mélange homogène. L’air est un mélange constitué de 78 % de diazote, 21 % de dioxygène et 1 % d’autres gaz.
La proportion en masse d’une espèce E dans un mélange est m(E)mtotale avec m(E) et mtotale exprimées dans la même unité.
La proportion en volume d’une espèce E dans un mélange est V(E)Vtotale avec V(E) et Vtotal exprimées dans la même unité.
Si ces rapports sont exprimés en %, on parle de pourcentage massique et pourcentage volumique.
Exemple : Pm(E)=m(E)mtotale×100
On peut identifier un corps pur grâce à :
- sa masse volumique ρ, en g.L−1 sachant que la masse volumique est caractéristique d’une espèce : ρ=mV avec m masse de l’espèce en g et V volume de l’espèce en L.
- sa densité sans unité : dcorps=ρcorpsρeau avec ρeau=1 kg.L−1=1 g.mL−1.
- des tests de reconnaissance
Test de reconnaissance de l’eau : le sulfate de cuivre anhydre (blanc) devient bleu en présence d’eau.
Test de reconnaissance du dioxyde de carbone : L’eau de chaux se trouble (blanchit) en présence de dioxyde de carbone.
Test du gaz dihydrogène : une allumette enflammée placée à l'orifice d'un tube contenant du dihydrogène provoque une légère détonation.
Test du gaz dioxygène : ce gaz ravive ou rallume une bûchette présentant un point d'incandescence. - un changement d’état à température constante
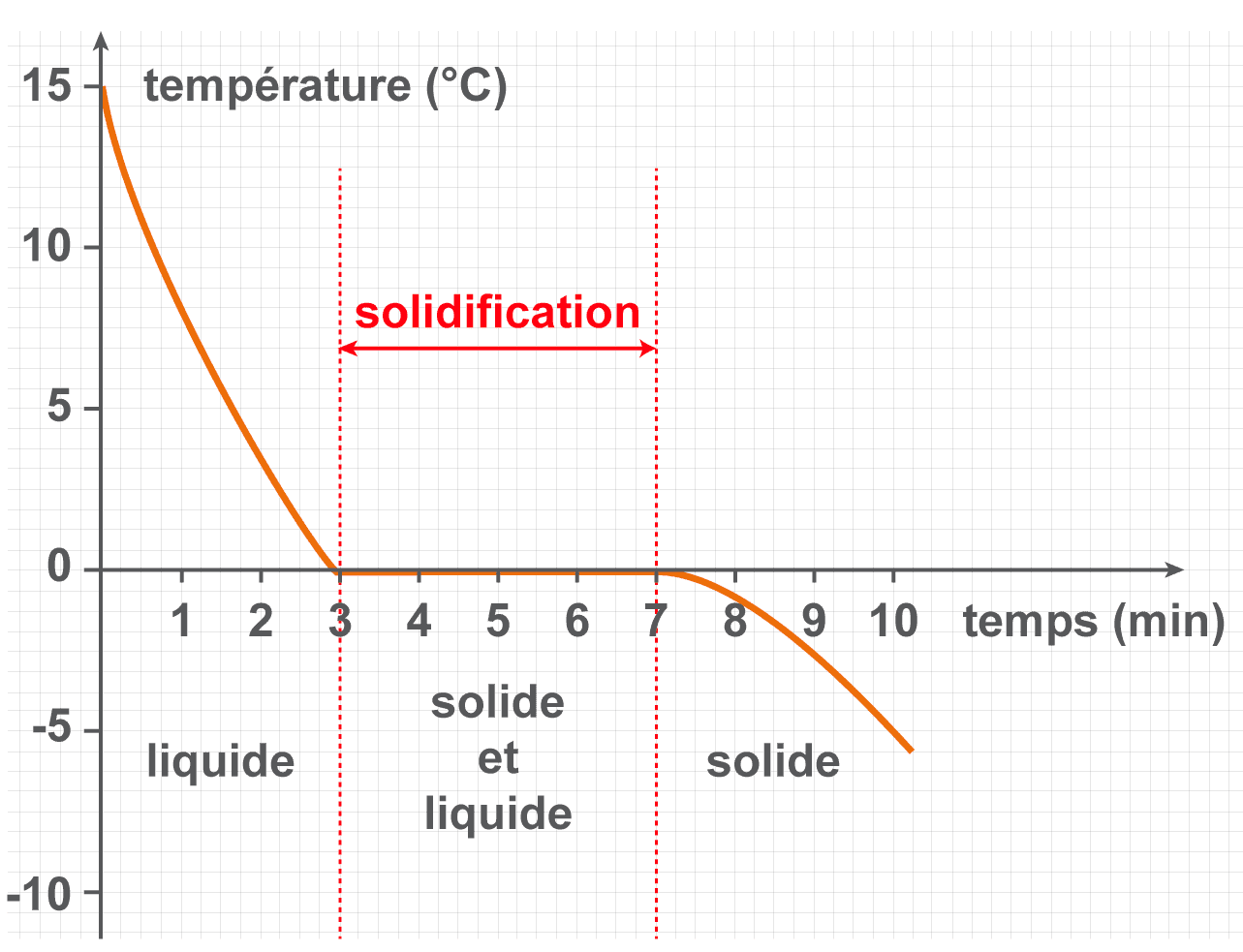
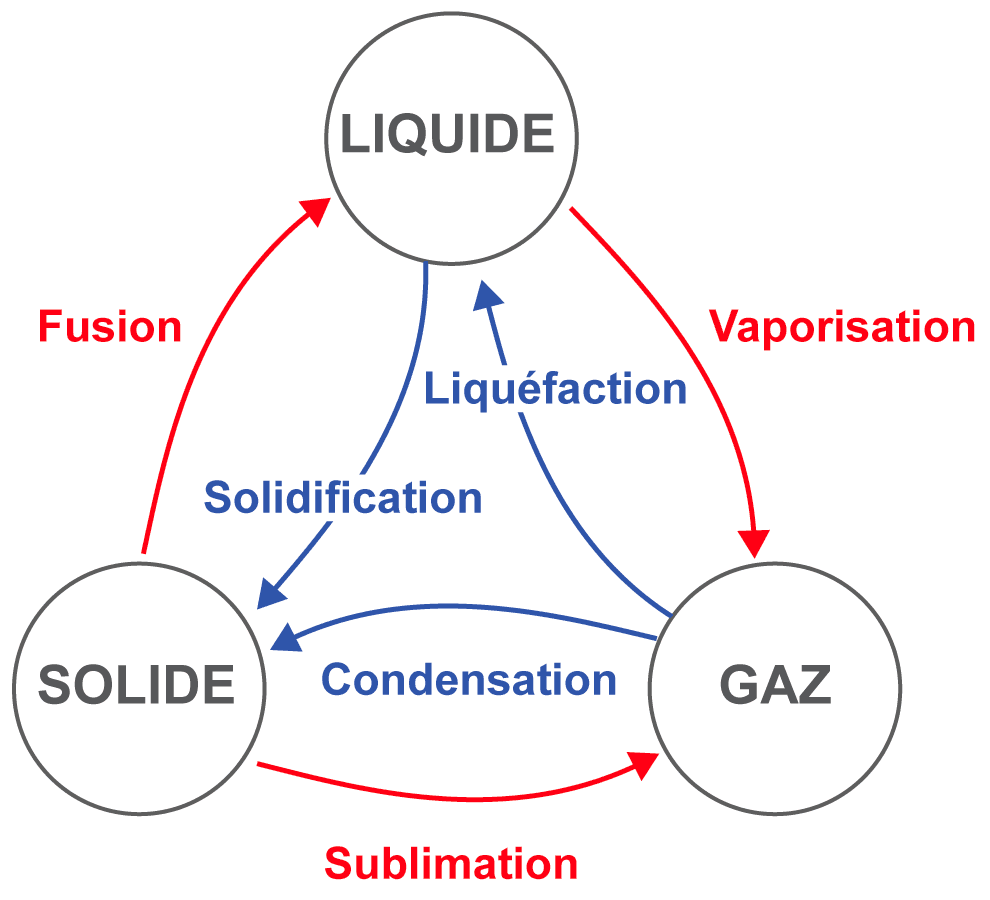
- On peut aussi réaliser une chromatographie sur couche mince (CCM) qui permet de séparer et d’identifier des espèces chimiques
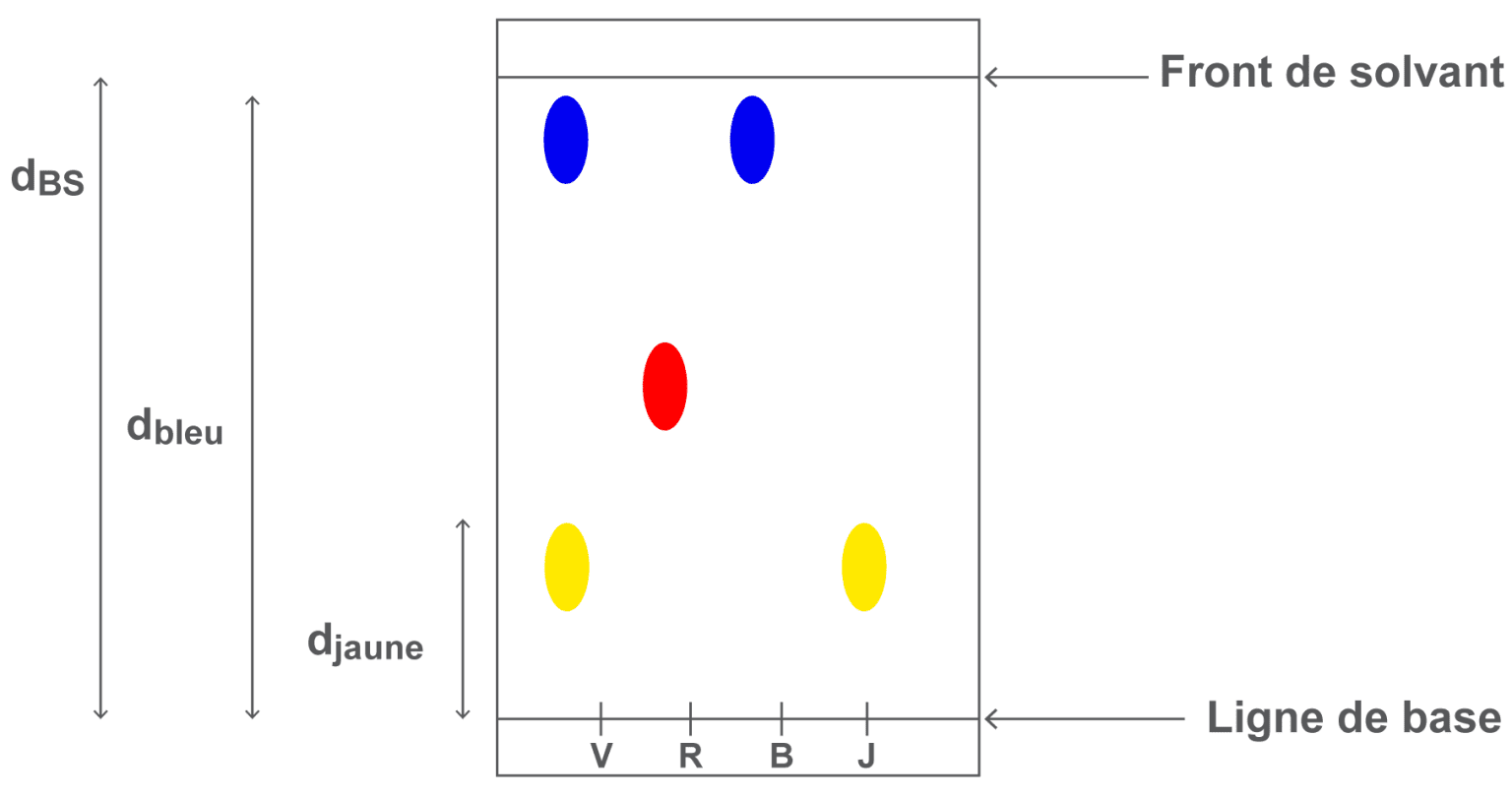
V a une tache à la même hauteur que J donc V contient J.
De même, V contient B.
V est un mélange (2 taches).