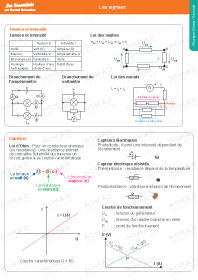
Des isotopes d’un élément ont un même nombre de protons mais un nombre de neutrons différents. Ils ont donc le même numéro atomique Z mais des nombres de masse A différents.
Une réaction nucléaire est une transformation d'un ou plusieurs noyaux atomiques. Elle se distingue d'une réaction chimique, qui ne concerne que les électrons ou les liaisons entre les atomes.
La réaction chimique conserve les éléments, alors que la réaction nucléaire transforme un élément en un autre.
Au cours d’une transformation nucléaire il y a conservation du :
- nombre de charge Z
- nombre de masse A
Exemple :
21084Po→ 20682+ 42He