Énergie d’un photon
📝 Mini-cours GRATUIT
Absorption d’un photon par un atome
Émission de la lumière par un atome
🍀 Fiches de révision PREMIUM

Énergie chimique
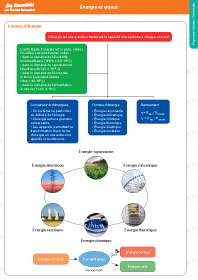
Énergie et enjeux

Les propriétés des matériaux et l'organisation de la matière

Énergie transportée par la lumière

Énergie mécanique

Les réactions acido-basiques

Les réactions d'oxydoréduction

Travail d'une force
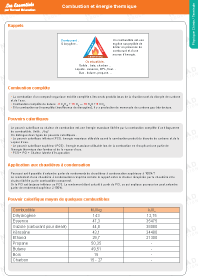
Combustion et énergie thermique



